Каква е конфигурацията на електрон
Електронни конфигурация атом - разпределението на електрони над енергийните нива и поднива. За конвенционална запис електронен конфигурация използва електронни формули.
Електронен представлява формула, основана на принципа на минимална енергия и принципи Паули, като се използва следния алгоритъм:
за всяка точка на броя на електрон енергийно ниво с помощта на цифровата стойност на основната квантовата числото п (виж Таблица 3.6.);
посочва енергия подниво чрез буквено орбитално квантово число л (виж Таблица 3.6.);
посочете общия брой на електроните в енергийния подниво с малки номера, който е написан в горния десен ъгъл над азбуката орбитална квантово число л.
Например, записване 1s1 - Е е формула в която малък брой означава един електрон, което е първото ниво на енергия (п = 1), S-подслой (л = 0). Следователно формула електронен отразява електронен конфигурация елемент водороден атом Н, където има един електрон.
Електронни конфигурация 21Sc член скандий атом, където има електрон 21 могат да бъдат написани д 1s22s22r63s23r64s23d1 формула или в друга форма, сумиране всички поднива в съответните енергийни нива:
От електрон формула 21Sc елемент атом може да се види, че черупката електрони включва два електрона S-подслой на първото ниво на енергия (1s2), два електрони S-подниво и шест електроните на нивото на втори енергия р-подслой, т.е. осем електрони на второ ниво ( 2s22r6), два електрони S-подслой, шест електрони на р-подслой, един електрон на трето ниво г-подниво енергия, т.е. девет електрони при трето ниво на енергията (3s23r63d1) и два електрона S-четвърто подслой енергийни URS I (4s2).
Понякога за улесняване електронни формули вместо вътрешна електронни слоеве атом символ написани в скоби преди инертен елемент. Най-близкото предшестващо на скандий 21Sc инертен елемент е аргон 18Ar обаче кондензира формула Е има формата на скандий
За атом могат да образуват електрон-блок-схема, която показва разположение на електроните в квантовите клетките показващи орбити. С оглед на принципа на минималната енергия се поставя в долната част на първото ниво на енергия клетка-орбиталния (п = 1), над него - втората (п = 2), а след това - на третия (п = 3), и т.н. електронен блок-схема на един атом на скандий 21Sc показано както следва:
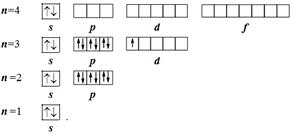
Използвайте и намалени електрон графики, които показват квантов клетка само външни електронни слоеве. Броят им се определя от местоположението образуване на електрона, който е, че електрон който изпълва последната електрони обвивка на атома. За скандий атом образуване на електрона (№ 21), разположени на 3d-подслой, така кондензирано електронен блок-схема трябва да показва две нива:
В зависимост от енергия подниво електрон постъпва формоване, елементите са разделени на S-, р-, d- и е-е-семейство комбиниране s-, р, D- и F-елементи, съответно.
Елементите в атоми, която се пълни S-подслой ниво външна енергия, наречени S-елементи.
Например, литий и берилий са S-елементи:
Елементите в атоми, която се пълни с р-подслой на външния слой, наречен Р-елементи.
Например, елементите въглерод и неонови са р-елементи:
Елементите в атоми, която се пълни г-втората подслой върху външната страна на нивото на енергия, наречени г-елементи.
Например, десет елемента - от скандий на цинк - принадлежат към семейството на г-е и г-елементи са, защото техните електрони образуващи атоми са на г-подниво:
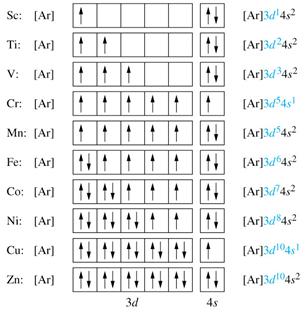
Елементите в атомите, на които се запълват с F-подслой върху външната страна на третия слой, наречен F-елементи.
Например, церий елементи и протактиний са F-елементи:
Пример 3.11. Направи имейл формула и електрон - блокова схема, два външни енергийни нива за такива частици: а) Аг атома; б) S2- йон; в) йон К +; ж) йони Zn2 +. Посочва изоелектронни частици.
Решение. Изоелектронен наречен частици, които имат една и съща електронна конфигурация, така че тяхната структура е описано от същите формули и същите модели електронен електронни дифракционни.
а) брой елемент аргон последователност (18) показва, че Аг атом има 18 електрони; местоположение в третия период - наличието на трите енергийни нива, като в осмата група - броя на външно ниво електрон равно на осем и основната подгрупа (VIIIA) показва Аг, принадлежащ към семейството на р-електрон. Следователно, електрон и електрон формула графиката за двата външни слоя от аргон атома елемент има формата
б) Номер на химичен елемент сяра S е 16, така електрон формула S атом
Въпреки това, йонен заряд (-2) показва, че в йон S2- два електрона пред S, т.е. атом 16 + 2 = 18. Поради същия брой електрони атом и Аг йони са изоелектронни S 2 'частици и има същата формула и електронни катод графиките на:
в) Брой на калиев химичния елемент - 19, така че К атом съдържа 19 електрони и йони К + - един електрон-малка (19-1 = 18). Следователно, К + йон е изоелектронен по отношение на частиците атом и Аг йони S2-, което е видно от формула Е к + йон и електрон - графичен схема:
ж) Ion Zn2 + (№ 30) има два електрона по-малко от цинк атом, така че Zn2 + йон размер на електрони е 30-2 = 28. поставянето им в електронна обвивка е описано с формулата Е
и електронен блок-схема две външни енергийни нива има формата
Следователно, Zn2 + йон не е изоелектронен частиците Аг атом и К + и S 2 'йони.
Ключови думи и термини
Какво е електронен конфигурацията на атомите, електроните формула?
Какво елементи се наричат: а) S-елементи; б) р-елементи; а) г-елементи;
Задачи за самостоятелна работа
Какво електронен формула отговаря атом Br:
а) 1s22s22r63s23r64s24r5; б) 1s22s22r63s23r64s23d104r5; в) 1s22s22r63s23r64s24r65s24d5; ж) 1s22s22r63s23r64s24r65s24d4?
Направи електронни формули за атома с атомни номера на елементи: а) 5; б) 7; в) 9; г) 12; г) 16; д) 21; ж) 23; з) 30.
Последно електрон (образуващи) елемент, атом е описано от квантово число: п = 4, л = 1, m = 0, S = + 1/2. Какво е елемент: а) Ga; б) Ti; а) Ge; ж) Са?
Последно електрон (образуващи) елемент, атом е описано от квантово число: п = 3, L = 2, т = - 1, и = -1 / 2. Какво този елемент: а) Fe; б) Co; а) Ni; ж) Na?
Последно електрон (образуващи) в атома на елемента е описан от номерата на квантовата:
а) п = 3, л = 1, m = - 1, S = - 1/2; б) п = 2, L = 0, m = 0, S = + 1/2; а) п = 3, L = 2, т = + 2,
S = + 1/2; ж) п = 3, L = 0, m = 0, S = + 1/2; г) п = 3, L = 0, m = 0, S = - 1/2.
Направи електронен формула на всеки елемент на атома.